Tienes que estudiar la Tabla Periódica, pues hoy es tu día de suerte aquí encontraras la mejor guía para hacerlo. Fácil intuitivo y rápido, así que empecemos.
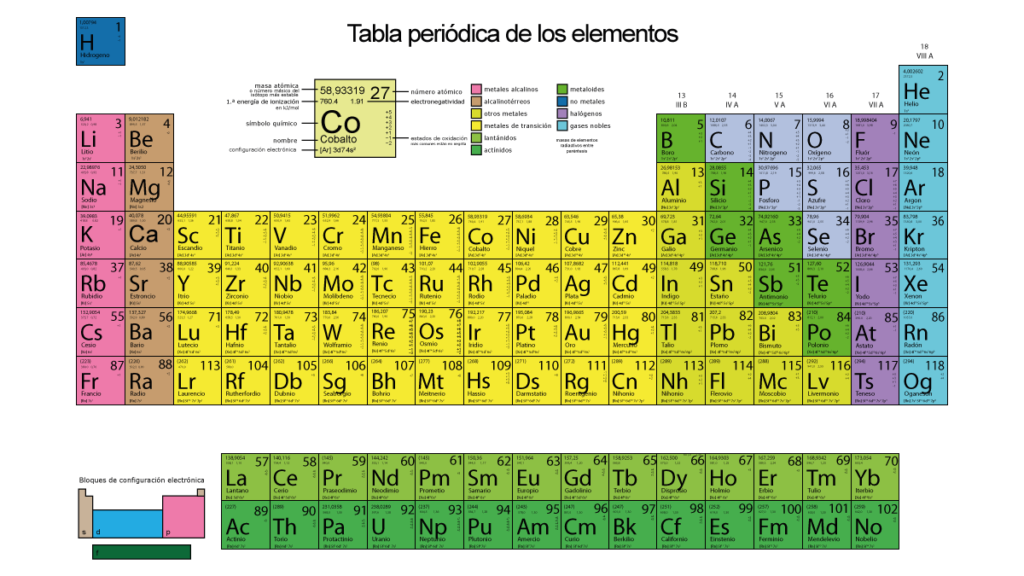
Tabla Periódica de los Elementos para Imprimir
Grupos y Periodos
La tabla periódica es una tabla donde se ordenan y clasifican todos los elementos.
Como toda tabla tiene filas y columnas, solo que aqui a las filas se les llama periodos y a las columnas grupos.
Los Periodos se representan con numeros y van del 1 al 7.
Los Grupos en cambio tienen 2 formatos uno que es completamente numérico y va del 1 al 18 y otro que es una combinación de una letra A o B seguida de un numero Romano.
A su vez dentro de la tabla hay grupos o familias de elementos donde están agrupados según propiedades y características (Propiedades Periódicas).
- Metales Alcalinos
- Metales Alcalinoterreos
- Metales
- Metaloides o Elementos de Transición
- No Metales
- Gases Nobles
- Lantánidos (Radiactivos)
- Actinidos (Radiactivos)
- Elemento
Elementos en la tabla periódica
Dentro de la tabla periódica cada elemento ocupa una celda pero antes que nada expliquemos que es un elemento.
Los elementos son categorías únicas que clasifican los átomos de una sustancia simple por su numero atómico.
Las celdas de cada elemento nos brindan información. Como por ejemplo, Símbolo, Numero Atómico, Numero Másico, estados de oxidación y configuración electrónica.
Su posición dentro de la tabla nos proporciona otros datos. como por ejemplo electronegatividad, radio atómico y su valencia.
Vamos a hacer un repaso general y luego vamos a ver punto por punto en profundidad. Muchos de los ejercicios de química se basan exclusivamente en saber interpretarla. Así que no dejes de ver esta Guía hasta el final.
Tanto el numero como el símbolo atómico es único para cada elemento.
El numero atomico y el masico aumentan de forma creciente de izquierda a derecha y de arriba hacia abajo.
mientras que el numero atomico representa la masa.
Por el contrario la electronegatividad crece de izquierda a derecha pero de arriba hacia abajo.

Metales y No Metales
Dentro de la tabla encontramos 2 grandes grupos fácilmente diferenciables, metales no metales
y los metales de transcicion o metaloides.
Los metales se encuentran a la izquierda y son electropositivos es decir tienen baja electronegatividad es por eso que son buenos
conductores del calor y la electricidad. Por el contrario los no metales son electronegativos, malos conductores y se encuentran
a la derecha. En el medio, justo entre los metales y los no metales se encuentran los metaloides o metales de trancicion.
estos tienen propiedades intermedias entre los metales y los no metales y tienden a comportarse segun con quien esten asociados.
por ejemplo si se asocian a un no metal mas electronegativo actuaran como metal y viseversa si se asocian a un metal electropositivo actuaran como no metal.
Valencia y Estados de Oxidación en la tabla periódica
Los estados de oxidacion nos indican que carga adoptaran los elementos al combinarse unos con otros. Puden tener carga negativa o positiva. Para poder recordarlos algunos los tendremos que memorizar pero muchos de ellos se pueden deducir por su posicion en la tabla la cual nos indica la valencia.
La Valencia nos indica cuantos electrones tiene el elemento en la ultima capa y esto en muchos casos nos permite deducir fácilmente el o los posibles estados de oxidación. por ejemplo sabiendo que un metal alcalino es muy electropositivo y tiene valencia 1 su estado de oxidación mas probable es +1.
Para aprenderlos los docentes suelen dejar trabajar a sus alumnos con una tabla muda. Una versión de la tabla en la que faltan algunos datos incluidos los números de oxidación.
Algunos docentes tienen la costumbre de obligar a sus alumnos a recordar los símbolos atómicos lo cual me parece mala idea. Lamentablemente la única forma de lograrlo es de memoria o usando reglas memotecnicas. actualmente estoy trabajando en un juego interactivo online como alternativa para aprenderla de forma mas fácil.