La estructura de lewis es una representacion grafica donde se puede observar los electrones de la ultima capa, cantidad y tipo de enlaces entre los elementos representados .
En esta web podrás aprender de manera muy sencilla tanto a leerlas como a realizarlas.
A continuación te mostraremos ejemplos ordenados por grado de complejidad y desarrollaremos cada uno paso a paso:
Estructura de Lewis, Ejercicios:

Estructura de Lewis O2
Ejercicio resuelto

Estructura de Lewis HCN
Ejercicio resuelto

Estructura de Lewis SO2
Ejercicio resuelto

Estructura de Lewis NH3
Ejercicio resuelto
Ejercicio: Representa la estructura de Lewis del O2:
Empezaremos con lo mas sencillo de menor a mayor.
Estructura de Lewis del O2:
Paso 1:
Escribe el simbolo atomico de los elementos de forma simetrica y con el elemento mas electronegativo en el Centro.
Simétricamente significa que si das vuelta el orden se ve igual. Al ser dos átomos de un mismo elemento se ve igual en cualquier caso. pero lo veras mejor en ejercicios mas avanzados y aun ahí seguirá siendo muy fácil.
Al ser dos átomos y de un mismo elemento, ambos son igual de electronegativos, así que por ser un ejemplo muy sencillo no habrá mayor dificultad con esto.

Paso 2:
Coloca los electrones de la ultima capa de cada uno y cuidaras que queden cercanos uno de otro los que intervienen en la unión. El oxigeno tiene 6 electrones en la ultima capa y los electrones que intervien en la union son 4 (dos pares) , te diremos a continuación como obtener estos datos.

Electrones en la ultima capa: Para saber cuantos son, debes fijarte en la tabla periódica, el grupo del elemento. Si el formato esta en números romanos, ese sera el valor, pero si esta en números decimales, es el valor del ultimo decimal. podrás verlo mas fácilmente en la imagen a continuación. Los electrones en la ultima capa de valencia son 6 por cada oxigeno.

Electrones que intervienen en la unión:
Ok, para saber cuantos electrones intervienen en la unión, debes hacer el siguiente ejercicio:
calcula cuantos electrones se requieren para completar el octeto electrónico de los ambos elementos . si aun no sabes lo que es octeto electronico, revisa el apartado Ley del Octeto. Se requieren 16 electrones (8 por cada átomo)
Los electrones disponibles son 12 (6 por cada átomo)
Bueno, ahora tienes que restar los electrones disponibles a los electrones necesarios para completar el octeto.
16e – 12e= 4e
El resultado es 4 electrones enlazantes (2 pares).
Normalmente para representar a los electrones se usa círculos para unos y cruces para el otro.
Quedaria entonces de esta manera:

Paso 3:
Ahora hay que enlazar los electrones hazlo con un circulo, un electrón enlazado de uno, cuenta como uno de otro y la suma debe dar ocho.

Chequeamos uno, y da 8 perfecto:

Chequeamos el otro y también da 8, genial:
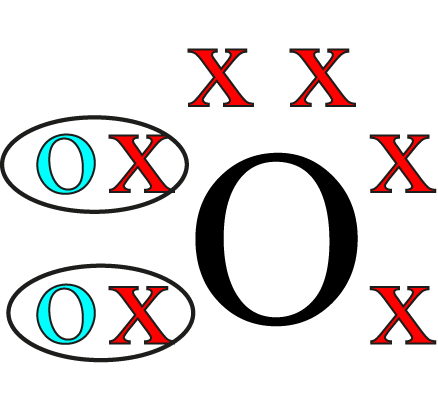
Listo ya tenemos nuestra primera estructura de Lewis (Recuerda que este es el ejemplo mas sencillo:
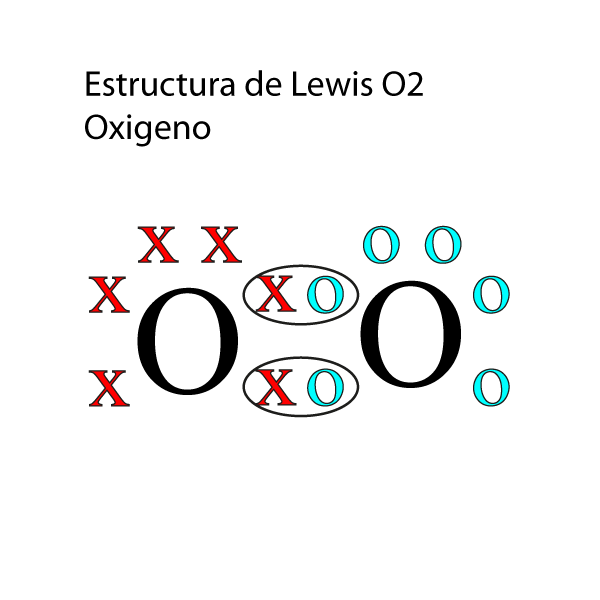


Ejercicio: Representa la estructura de Lewis del N2
Ok bueno ahora hagamos un ejercicio del Nitrogeno, N2:
Paso 1
Ordenamos simétricamente, son dos Nitrógenos, así que en este caso da igual.

Debemos colocar los electrones de la ultima capa de valencia y colocar entre ellos los electrones que intervienen en la union.
Buscamos en la tabla periodica cuantos electrones hay en la ultima capa de valencia de cada nitrogeno, como pertenece al grupo “V” o 15 ( segun el formato de la tabla) nos indica que tienen 5
Ahora calculamos los electrones que intervienen en la union. Cada Nitrogeno tiene 5 electrones en su capa de valencia, entre los dos suman 10 y necesita 16 electrones para completar el octeto electronico de ambos.
16e – 10e= 6e (electrones enlazantes, 3 pares)
ahora que sabemos que cada Nitrogeno tiene 5 electrones en su ultima capa de valencia y que se unen entre si por 3 pares, los colocaremos de esta forma:

paso siguiente, enlazar los electrones, marcalos con un circulo, cada electrón unido de un nitrógeno, cuenta como uno de otro y el total debe dar ocho.
El primer nitrogeno tiene 8e, Genial!!

El segundo tambien, Fantastico!!

Listo ya tenemos la estructura de lewis del nitrogeno completa:
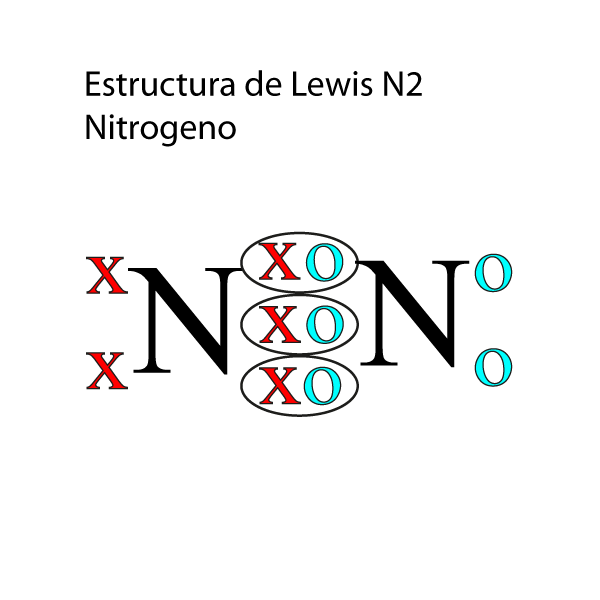


Ejercicio: Representa la estructura de Lewis del NO
Ok bueno ahora hagamos un ejercicio del NO, Monoxido de Nitrógeno.
Este ejercicio tiene una peculiaridad, por lo cual deberás prestar mayor atención. En el NO, Monoxido de nitrógeno, no se cumple la ley del octeto. En esta web veras varios ejemplos y te haremos saber cuando esto ocurra.
Continuemos entonces con el ejercicio, Ordenamos simétricamente, para este caso es lo mismo.

coloca los electrones de la ultima capa de valencia y coloca entre ellos los electrones que intervienen en la unión.
Buscamos en la tabla periodica cuantos electrones hay en la ultima capa de valencia del nitrogeno, como pertenece al grupo “V” o 15 ( segun el formato de la tabla) nos indica que tiene 5. ahora nos fijamos igual cuntos hay en la del oxigeno, como pertenece al grupo “VI”A o 16 (segun el formato) entendemos que son 6
Ahora calculamos los electrones que intervienen en la union. El Nitrogeno tiene 5 electrones en su capa de valencia y el oxigeno 6, entre los dos suman 11 y necesita 16 electrones para completar el octeto electronico de ambos.
16e – 11e= 5e ( Los electrones se unen de a pares) No se puede cumplir ley del octeto. por consiguiente se enlazan tantos pares de electrones como sea posible (osea 4 electrones, dos pares)
ahora que sabemos que el Nitrogeno tiene 5 electrones en su ultima capa, el oxigeno 6, y que se unen entre si por 2 pares, los colocaremos de esta forma:

paso siguiente, enlazar los electrones, marcalos con un circulo. Cada electrón unido , cuenta como uno de otro y como veraz no hay forma en la cual ambos elementos.
Contamos y da 7e (no es lo ideal, pero es la forma mas estable que puede obtener)

Contamos efectivamente los del oxigeno y estos si dan 8:

y asi queda, en fin, no se cumple la ley del octeto para todos los elementos pero esta es la estructura mas estable que se puede obtener:


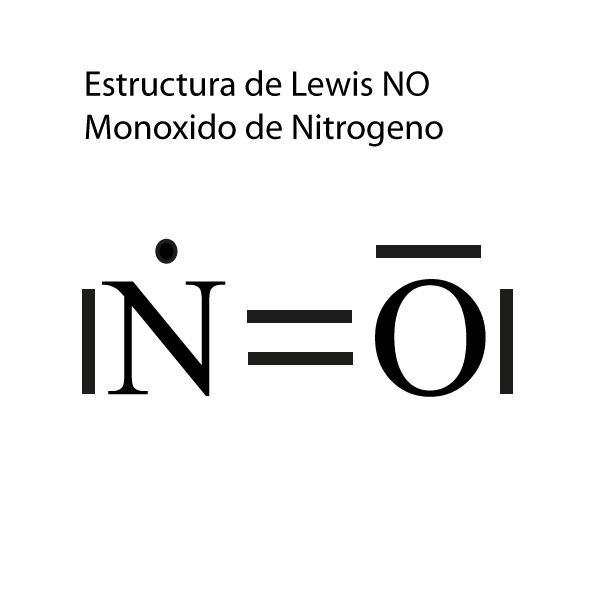
Que no se cumpla la ley del octeto, no es habitual, pero si sucede en varios casos. Te recomendamos que veas los siguientes ejemplos:
Ok bueno ahora hagamos un ejercicio del monoxido de Carbono o CO :








