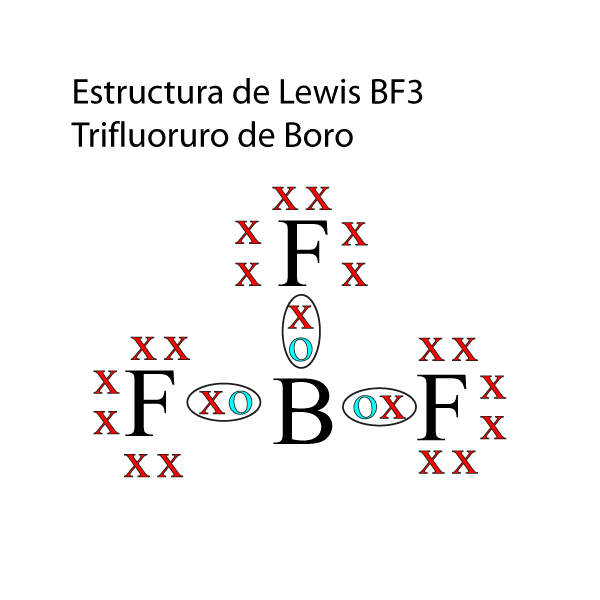


A continuación desarrollaremos paso a paso la estructura de lewis del BF3
Estructura de Lewis BF3, Ejercicio:
Primero ordenamos simétricamente asegurándonos que el elemento menos electronegativo quede en el centro. Como podemos observar en la tabla periódica el elemento menos electronegativo es el boro, los elementos entonces se ordenan de esta forma:

Antes que nada hay que aclarar una cosa, en el caso del BF3, no se cumple la ley del octeto, esto no es habitual pero existen excepciones como esta y es bueno que lo sepas.
Escribe los electrones de la ultima capa de valencia de cada uno de los elementos constatando que queden cercanos unos de otros los que interactúan en la unión.
Veamos lo en la tabla periodica.
Buscamos en la tabla periódica cuantos electrones hay en la ultima capa de valencia del Flúor, como pertenece al grupo “VII” o 17 ( según el formato de la tabla) nos indica que tiene 7. ahora nos fijamos igual cuantos hay en la del Boro, como pertenece al grupo “III”A o 13, entendemos que son 3.
Atomos requeridos para completar el octeto: 8×3 para cada fluor + 8 para el boro= 32e
electrones disponibles en la ultima capa: 3 del boro y 7 por cada fluor (21)=24
32-24=8e (4 pares), esto no se cumple debido a que el boro solo tiene 3 electrones en su ultima capa y como los enlaces comparten un electron de cada uno solo se pueden formar 3 pares, como ya mencionamos en este caso no se cumple la ley del octeto.
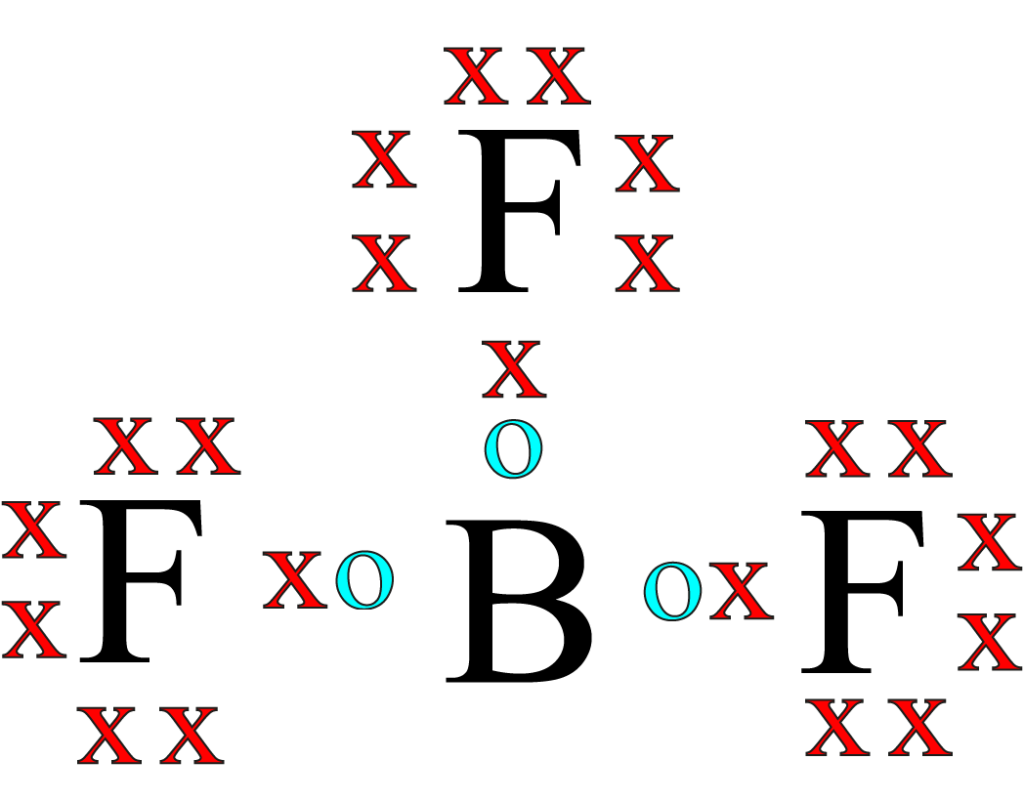
Podemos verificar que la ley del octeto se cumple en los 3 atomos de fluor no asi en el boro que queda con 6 electrones en su ultima capa de valencia.
En los tres átomos de flúor se cumple la ley del octeto:

No asi en el caso del Boro:

Como vimos anteriormente se pueden formar solo 3 pares de enlaces, marquemos los con un circulo y la estructura de lewis final nos quedara terminada.
Ahora hagamos la estructura de lewis del NO2:
O tal vez prefieras hacer la Estructura de lewis del CO: